|
Vernacular Name
Rana terrestre común
State/Provinces
Morona Santiago, Orellana, Pastaza, Sucumbíos, Zamora Chinchipe
Natural Regions
Bosque Húmedo Tropical Amazónico, Bosque Piemontano Oriental
Identification
Es una rana mediana de color café, superficie posterior de los muslos con líneas claras y vientre crema amarillento con moteado gris hacia el tercio anterior del cuerpo. Presenta rebordes cutáneos en los dedos del pie. En la Amazonía de Ecuador, Leptodactylus leptodactyloides se asemeja más a Leptodactylus wagneri. Leptodactylus wagneri se diferencia por su mayor tamaño ( LRC promedio = 50.4 mm en machos y 66.4 mm en hembras, 19). Además, generalmente, la coloración ventral de Leptodactylus wagneri tiene moteado gris en todo el vientre (moteado restringido al tercio anterior del cuerpo en Leptodactylus leptodactyloides). Se diferencia de Leptodactylus petersii por tener la superficie posterior de muslos con líneas claras (ausentes en Leptodactylus petersii) y vientre crema amarillento con moteado gris hacia el tercio anterior del cuerpo (vientre uniformemente moteado con manchas más grandes y a menudo con un patrón anastomótico en Leptodactylus petersii) ( 4, 10). Se diferencia de Leptodactylus discodactylus por ser más grande ( LRC < 35 mm en Leptodactylus discodactylus) y por la ausencia de discos moderadamente expandidos en la punta de los dedos del pie (presentes en Leptodactylus discodactylus). Se diferencia otras especies simpátricas de Leptodactylus ( Leptodactylus knudseni, Leptodactylus pentadactylus, Leptodactylus rhodomystax, Leptodactylus stenodema, Leptodactylus stenodema) por la presencia de rebordes cutáneos en los dedos del pie (ausentes en las especies mencionadas). Se diferencia de Adenomera por ser más grande ( LRC < 29 mm en Adenomera), tener el Dedo I más largo que el Dedo II en la mano (dedos iguales en longitud en Adenomera), rebordes cutáneos en los dedos de los pies (ausentes en Adenomera) y su coloración ventral (vientre totalmente blanco en Adenomera). Otras especies simpátricas con las que Leptodactylus leptodactyloides puede resultar similar son craugastóridos ( Pristimantis) y ránidos ( Rana). Se diferencia de la mayoría de Pristimantis por su vientre liso y por carecer de discos expandidos en los dedos (vientre areolado y discos presentes en Pristimantis). Se diferencia de Rana por carecer de membranas entre los dedos del pie (membrana extensa en Rana; modificado de Duellman ( 2)).
Description
Es una rana de tamaño mediano con la siguiente combinación de caracteres (modificado de Andersson (1) Heyer (4)): (1) en vista dorsal, cráneo tan largo como ancho; canto rostral redondeado, indistinto; región loreal vertical, ligeramente cóncava; (2) tímpano distinto, ligeramente más grande que la mitad del diámetro del ojo; pliegue supratimpámico presente y glandular; hinchamiento glandular presente detrás del ángulo de la mandíbula; (3) superficies dorsales finamente ásperas, a excepción de cabeza y región anterior del dorso que son lisas, región posterior de dorso con espículas puntiagudas, algunas también presentes en superficie dorsal de muslos; pliegues dorsolaterales presentes, irregulares y poco conspicuos, rara vez son largos y distintos; flancos, vientre y superficie posterior y ventral de muslos granular, siendo más lisa en garganta y pecho; superficie ventral de extremidades lisa; (4) Dedo I más grande que Dedo II en la mano; puntas de dedos engrosadas pero no dilatadas; tubérculos subarticulares puntiagudos; machos tienen dos espinas negras de tamaño medio en el pulgar; (5) dedos del pie largos; membrana basal entre los dedos del pie; rebordes cutáneos presentes; pliegue tarsal presente.
Color in Life
Modificado de Andersson (1) y Heyer (4): (1) Presenta barras verticales obscuras usualmente indistintas en el labio superior, las barras posteriores se extienden hasta la esquina posterior del ojo; (2) dorso café obscuro; banda ancha transversal en forma de semi-luna se extiende desde los párpados y está presente entre los ojos y la parte anterior del cuello; barras anchas transversales obscuras presentes en superficie dorsal de muslos y tibia; (3) vientre, parte ventral de flancos y pecho crema amarillentos con un patrón finamente moteado gris obscuro en el tercio anterior del cuerpo; (4) superficie ventral de extremidades café uniforme, a excepción de la superficie ventral y posterior de muslos que lleva líneas claras distintas, o al menos una indicación de las mismas.
Males Face Cloacal Length Average
Promedio = 40.1 mm (rango 28.3–47.9; n = 235). Promedio para la Amazonía ecuatoriana = 40.3 mm (rango 38.6-43.4; n = 4) (
Females Face Cloacal Length Average
Promedio = 46.3 mm (rango 34.8–56.2; n = 388). Promedio para la Amazonía ecuatoriana = 47.1 mm (rango 38.9-51.6; n = 6) (4, 19
Habitat and Biology
Leptodactylus leptodactyloides se encuentra en bosque primario y secundario, borde de bosque, sabanas y áreas abiertas, generalmente bajo troncos caídos (14). La reproducción ocurre en cuerpos de agua temporales. Los huevos son depositados en nidos de espuma; los renacuajos son exotróficos, se desarrollan en agua léntica (11, 14) y alcanzan una longitud de 28.3 mm (4). Leptodactylus leptodactyloides se encuentra en los mismos hábitats generales que Leptodactylus petersii, Leptodactylus mystaceus y Leptodactylus wagneri (4).
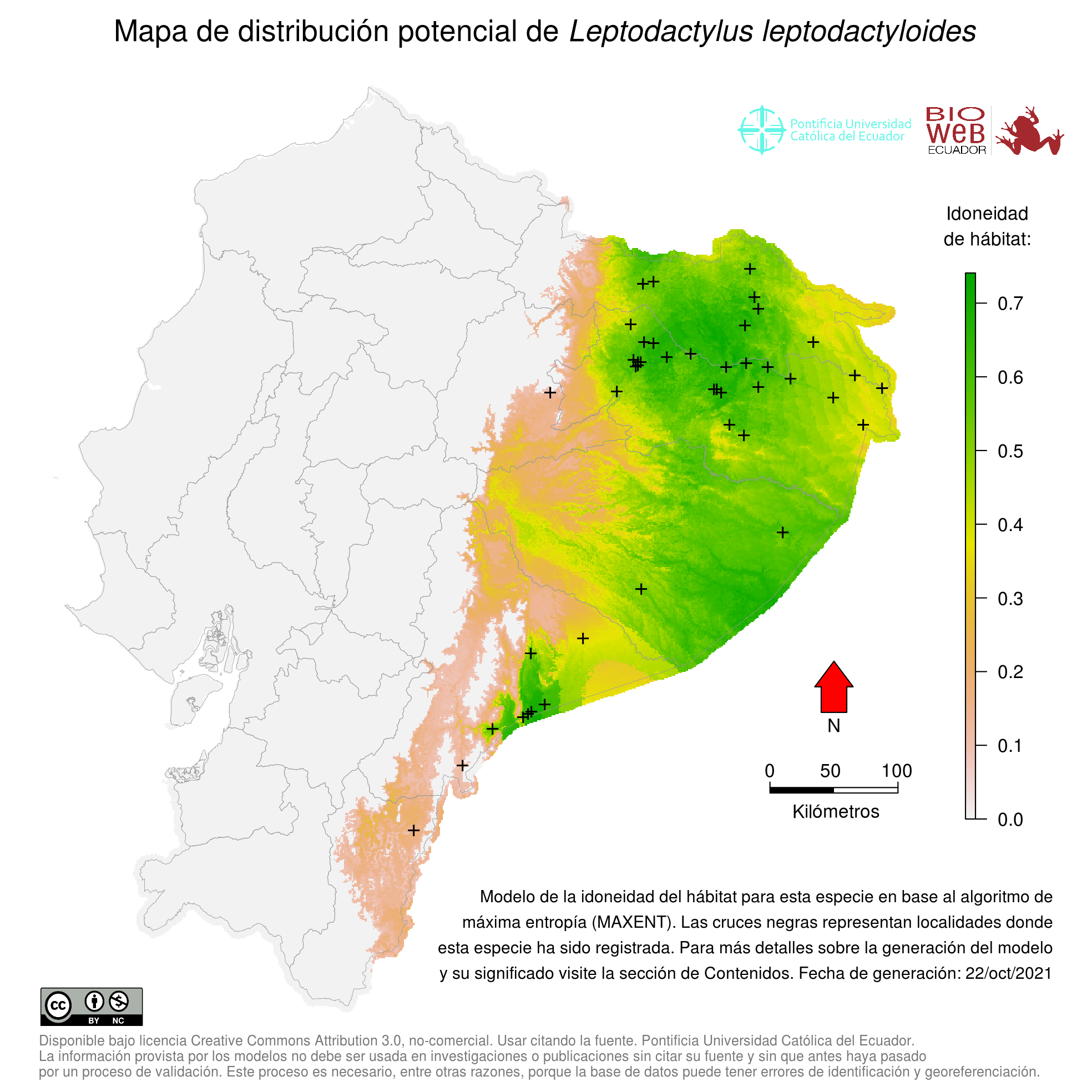
Distribution
Se distribuye en toda la Cuenca amazónica de Ecuador, Perú, Bolivia, Colombia, Venezuela, Brasil y en Guyana, Guayana Francesa y Suriname (4, 10, 14).
Altitudinal Range
De 0 a 1000 m sobre el nivel del mar (4; 19).
Taxonomy and Evolutionary Relationships
Está cercanamente relacionado a Leptodactylus natalenis. Forma parte del grupo de especies Leptodactylus melanonotus (4, 5, 10, 15, 17, 20)
Etymology
Su nombre se debe a que Andersson consideró al holotipo como una especie nueva del género Eleutherodactylus, pero que se asemejaba mucho a Leptodactylus.
Additional Information
Andersson (1) presenta una fotografía en vista dorsal del espécimen utilizado para la descripción. Heyer (4) describe el renacuajo (sin ilustraciones) y el canto de anuncio acompañado de oscilogramas o audioespectrogramas. Su frecuencia dominante es de 650-1600 Hz. La duración del canto es de 0.01-0.04 s con 3-5 pulsos parciales por canto. Aumento de la frecuencia a lo largo del canto. Estructura armónica presente o ausente. Lescure y Marty (7) proporcionan una fotografía y un relato de Guayana Francesa, mientras que Ouboter y Jairam (16) de Surinam. Köhler (6) presenta un relato general de Bolivia, pero probablemente corresponda a otra especie según Jansen et al. (17) (ver sección Taxonomía y relaciones evolutivas). Andersson (1) erróneamente la describió bajo Pristimantis (Eleutherodactylus en ese entonces) (3). Heyer (5) la sinonimizó bajo Leptodactylus wagneri, pero posteriormente, Heyer (4) la removió de esta sinonimia (5). De Sá et al. (10) presentan una filogenia basada en caracteres morfológicos y moleculares, en la cual ubican a Leptodactylus leptodactyloides como especie hermana de Leptodactylus chaquensis. Jansen et al. (17) considera que las poblaciones de Bolivia representan una especie morfológica y genéticamente distinta a Leptodactylus leptodactyloides de Brasil. Ambas especies son hermanas, y muestran una relación mas o menos cercana con Leptodactylus podicipinus y Leptodactylus wagneri (17). Por otra parte, la filogenia de Jansen et al. (17) no soporta una relación cercana con Leptodactylus chaquensis como fue propuesta por de Sá et al. (10).
Maxson y Heyer (13) realizan un análisis bioquímico de albúminas para varias especies de Leptodactylus, dando soporte a la distinción de los grupos de especies pentadactylus y melanonotus; y sugieren también que la mayor diversificación en Leptodactylus ocurrió durante el Paleoceno (65.5–55.5 millones de años). Heyer (18) propone una representación diagramática de las relaciones entre grupos de especies dentro de Leptodactylus e indican que el grupo melanonotus estaría más cercanamente relacionado con el grupo ocellatus. Heyer (18) y Prado et al. (11) postularon que Leptodactylus y Adenomera constituyen un grupo que ha experimentado transición desde el medio acuático hacia el terrestre, y que la gran diversidad de los sitios de oviposición de nidos de espuma que existe entre especies abarca un amplio rango de esta transición. Siguiendo este razonamiento, los grupos de especies desde el más primitivo al más derivado son: melanonotus más ocellatus (nido en la superficie del agua), pentadactylus (nidos en cavidades adyacentes al agua), fuscus (nidos en cámaras de incubación y larva acuática), y Adenomera (nidos en cámaras de incubación y larva no acuática). También existe una relación en reducir el tamaño de la puesta y aumentar el diámetro de los huevos conforme un grupo es más terrestre (18). Bogart (9) y Amaro-Ghilardi et al. (12) sugieren que la condición de 26 cromosomas es primitiva en Leptodactylus, y que los linajes más derivados experimentaron una reducción a 22 o 24 cromosomas; sin embargo, Heyer y Diment (8) indican que el uso de cariotipos en develar las relaciones filogenéticas en Leptodactylidae es de uso limitado, y tiene que ser usado en combinación con otros sets de datos.



Summary Author
Diego A. Ortiz, Morley Read, Andrea Varela-Jaramillo y Santiago R. Ron
Editor
Santiago R. Ron
Edition Date
2018-04-18T00:00:00
Update Date
2022-09-26T18:52:10.987
Literature Cited
Andersson, L. G. 1945. Batrachians from East Ecuador collected 1937,1938 by Wm. Clarke-MacIntyre and Rolf Blomberg. Arkiv för Zoologi. Kongliga Svenska Vetenskaps-Akademiens, Stockholm. Arnoldia, Zimbabwe 37:32143.PDF Duellman, W. E. 1978. The biology of an equatorial herpetofauna in Amazonian Ecuador. Miscellaneous Publications of the University of Kansas 65:1-352.PDF Heyer, W. R. y Peters, J. A. 1971. The frog Genus Leptodactylus in Ecuador. Proceedings of the Biological Society of Washington 84:163-170. Heyer, W. R. 1994. Variation within the Leptodactylus podicipinus-wagneri complex of frogs (Amphibia: Leptodactylidae). Smithsonian Contributions to Zoology 546:1-124.PDF Heyer, W. R. 1970. Studies on the frogs of the genus Leptodactylus (Amphibia: Leptodactylidae). VI. Biosytematics of the melanonotus group. Los Angeles County Museum Contributions in Science:1-48.PDF Köhler, J. 2000. Amphibian diversity in Bolivia: a study with special reference to montane forest regions. Bonner Zoologische Monographien 48:1-243. Lescure, J. y Marty, C. 2000. Atlas des Amphibiens de Guyane. Collect. Patrimoines Nat., Paris 45:138-139. Heyer, W. R. y Diment, M. J. 1974. The karyotype of Vanzolinius discodactylus and comments on usefulness of karyotypes in determining relationships in the Leptodactylus-complex (Amphibia, Leptodactylidae). Proceedings of the Biological Society of Washington 87:327-336. Bogart, J. P. 1974. A Karyosystematic Study of Frogs in the genus Leptodactylus (Anura: Leptodactylidae). Copeia 1974:728-737.PDF De Sá, R. O., Heyer, W. R., Camargo, A. 2005. A Phylogenetic Analysis of Vanzolinius Heyer, 1974 (Amphibia, Anura, Leptodactylidae): Taxonomic and life history implications. Arquivos do Museu Nacional, Río de Janeiro 63:707-726.PDF Prado, C. P. A., Uetanabaro, M., Haddad, C. F. B. 2002. Description of a new reproductive mode in Leptodactylus (Anura, Leptodactylidae) with a review on the reproductive specialization toward terrestriality in the genus. Copeia 2002:1128-1133.PDF Amaro-Ghilardi, R. C., Skuk, G., de Sá, R., Rodrígues, M. T. y Yonenaga-Yassuda, Y. 2006. Karyotypes of eight species of Leptodactylus (Anura, Leptodactylidae) with a description of a new karyotype for the genus. Phyllomedusa 5:119-133. Maxson, L. R. y Heyer, W. R. 1988. Molecular systematics of the frogs genus Leptodactylus (Amphibia: Leptodactylidae). Fieldiana, Zoology, New Series 41:1-13. IUCN. 2010. The IUCN red list of threatened species. http://www.iucnredlist.org/apps/redlist/search. (Consultado: 2010). Pyron, R. A. y Wiens, J. J. 2011. A large-scale phylogeny of Amphibia including over 2800 species, and a revised classification of extant frogs, salamanders, and caecilians. Molecular Phylogenetics and Evolution 61:543-583. Ouboter, P. E. y Jairam, R. 2012. Amphibians of Suriname. Brill. 388 pp. Jansen, M., Bloch, R., Schulze, A., Pfenninger, M. 2011. Integrative inventory of Bolivia’s lowland anurans reveals hidden diversity. Zoologica Scripta 40:567-583. Heyer, W. R. 1969. The adaptative ecology of the species groups of the genus Leptodactylus (Amphibia, Leptodactylidae). Evolution 23:421-428.PDF Ron, S. R. 2018. Base de datos de la colección de anfibios del Museo de Zoología (QCAZ). Versión 1.0. Pontificia Universidad Católica del Ecuador. Disponible en https://bioweb.bio/portal/ Gazoni, T., Lyra, M., Ron, S., Strüssmann, C., Baldo, D., Narimatsu, H., Pansonato, A., Schneider, R., Giaretta, A., Haddad, C., Parise-Maltempi, P., de Carvalho, T. 2021. Revisiting the systematics of the Leptodactylus melanonotus group (Anura: Leptodactylidae): Redescription of L. petersii and revalidation of its junior synonyms. Zoologischer Anzeiger 290: 117—134.
|





 Map of Life
Map of Life



