|
Vernacular Name
Sapo bocón del Pacífico
State/Provinces
Guayas, El Oro, Manabí, Santa Elena
Natural Regions
Matorral Seco de la Costa, Bosque Deciduo de la Costa
Identification
Se diferencia de todas las especies que habitan la región Costa del Ecuador por su cabeza y boca extremadamente anchas y marcas obscuras en sus superficies dorsales. Las marcas son bien definidas y altamente tuberculares especialmente hacia su periferia. La coloración dorsal varía entre café oscuro, café claro, verde claro y verde oscuro; las marcas tuberculares son siempre más oscuras. La presencia de espádices (estructuras en forma de pala) en la planta de los pies también es única entre los anfibios de la región Costa. Los espádices le permiten enterrarse en el suelo. Las especies más similares en Ecuador son las especies amazónicas Ceratophrys cornuta y Ceratophrys testudo de la que se diferencia por carecer de apéndices dérmicos en forma de cuerno sobre los ojos (presentes en las dos especies amazónicas) y tener los espádices queratinizados en los pies (espádices no queratinizados en Ceratophrys cornuta ni en Ceratophrys testudo) ( 4, 6).
Description
Presenta la siguiente combinación de caracteres ( 1, 5): (1) cráneo y boca muy anchos; (2) ausencia de apéndices dermales en el párpado superior; (3) tímpano visible, ovalado verticalmente, del tamaño de la mitad del ojo; borde supratimpánico pobremente definido; (4) hocico redondeado en vista dorsal y pronunciado hacia delante con una marcada pendiente desde las narinas hasta la punta en vista lateral; (5) mandíbula inferior ligeramente oculta bajo la mandíbula superior; mandíbula inferior con dos procesos óseos, ubicados medialmente hacia el interior de la boca; (6) presencia de una marca obscura interorbital; presencia de una marca alargada obscura que va desde el ojo, a través del canto rostral, hasta la punta del hocico; (7) procesos dentígeros de los vómers pequeños; (8) cuerpo rechoncho y pequeño en comparación a la cabeza; escudo óseo en el dorso ausente; (9) piel dorsal lisa, a excepción de marcas irregulares más obscuras con tubérculos; piel de los flancos y vientre lisa con granulación leve; superficie ventral y posterior de los muslos pustular; pequeño pliegue dérmico en el borde externo del pie; machos con saco vocal pareado; (10) extremidades anteriores robustas y cortas; Dedo I de la mano más largo que el Dedo II; dedos anchos y sin membrana; machos con excrescencias nupciales en la base del pulgar en época de reproducción; (11) extremidades posteriores robustas y cortas, con barras transversales más obscuras, con gránulos y pústulas; Dedo IV del pie casi del doble de tamaño que el Dedo V y algo mayor que el Dedo III; dedos unidos por una membrana rudimentaria que se extiende poco más allá de los tubérculos subarticulares basales; (12) estructura queratinizada metatarsal a manera de pala de color marrón obscuro a negro (recibe el nombre de espádice, presuntamente sirve para cavar y enterrarse).
Color in Life
Color dorsal variable de café claro, café obscuro a verde claro, verde obscuro y verde grisáceo; superficies dorsales con marcas alargadas y redondeadas bien definidas, irregulares y más obscuras (ej. marrón, café oscuro, negro) que el color de fondo, llevando numerosos tubérculos, estas marcas están delineadas por una línea más clara; vientre blanco grisáceo con algunas manchas pequeñas cafés ubicadas lateralmente; garganta con manchas obscuras irregulares (5).
Males Face Cloacal Length Average
Promedio = 57.5 mm (rango 48.4–67.9; n = 20). (8
Females Face Cloacal Length Average
Promedio = 67.6 mm (rango 53.1–82.0; n = 19). (8
Habitat and Biology
Ceratophrys stolzmanni habita los ecosistemas de matorral seco y bosque deciduo de la costa del Pacífico. La especie vive bajo tierra durante la mayor parte del año, y emerge durante el periodo de lluvias (enero–marzo) para reproducirse (11, 15). En una sola noche, en la época lluviosa de 2007, se colectaron 19 machos y 25 hembras (entre adultos y subadultos) en la Reserva Ecológica Militar Arenillas (REMA), Provincia El Oro, Ecuador. Estos individuos fueron encontrados en pozas temporales dentro del bosque y también en zonas más disturbadas (i.e. algunos árboles con suelo arado para agricultura) (8). El hábitat en Cuatro Hermanitos (Provincia Guayas, Ecuador) fue descrito como desierto abierto y arenoso, con vegetación baja y dispersa y árboles que están ausentes excepto en las cercanías de riachuelos temporales (5). En esta misma localidad, también se reportaron otros anuros como Rhinella bella, Rana sp. y la lagartija Stenocercus iridescens (5). Es una especie voraz que se alimenta de gran diversidad de animales y diferentes tamaños de presa (esta última variable no estuvo correlacionada con el tamaño de la rana) que incluyen invertebrados (arácnidos, insectos, gastrópodos, cienpiés) y vertebrados como ranas (Trachycephalus jordani, Leptodactylus labrosus) y serpientes (Leptodeira septentrionalis) (17). Se han documentado también casos de canibalismo (entre renacuajos y juveniles) y necrófagia (hacia otras especies de anuros) (8, 17). Esta estrategia comportamental de forrajeo (macrofagia), así como su rápido desarrollo como renacuajos y juveniles, aparentemente responderían a su ecología y la estacionalidad de sus ecosistemas (actividad de la especie restricta a pocos meses húmedos durante el año) (14, 15).
Reproduction
En una localidad en el sur de Ecuador, se reproducen entre febrero y marzo y alcanzan la metamorfosis entre marzo y abril (15). El tiempo reproductivo potencial es dos años para los machos y tres años para las hembras en promedio (15). Algunas puestas obtenidas en cautiverio promediaron 664 huevos (rango 200–2100; n = 9) y el desarrollo de estos renacuajos hasta alcanzar la metamorfosis fue rápido con un promedio de 25 días (rango 20–32; n = 10)(8). En estado natural, los renacuajos son capaces de abandonar las posas desde 16.5 días hasta 26 días después de la deposición de los huevos (14). Su desarrollo rápido aparentemente les permite a los renacuajos completar la metamorfosis antes que se sequen las pozas efímeras donde se desarrollan en estado natural (8, 14). Presentan un crecimiento rápido durante el primer año y alcanzan su madurez sexual antes del año de edad (8, 15). Al momento de la metamorfosis, los juveniles tienen una LRC promedio de 34.4 mm y un peso de 4.14 g. Luego de la metamorfosis, durante el primer año de vida, los machos aumentan su LRC 1.76 veces y las hembras 1.87 veces. La tasa de crecimiento disminuye substancialmente cuando alcanzan la madurez sexual (15). La longevidad es baja puesto que solo el 2% de los adultos alcanzan cuatro años de edad (15).
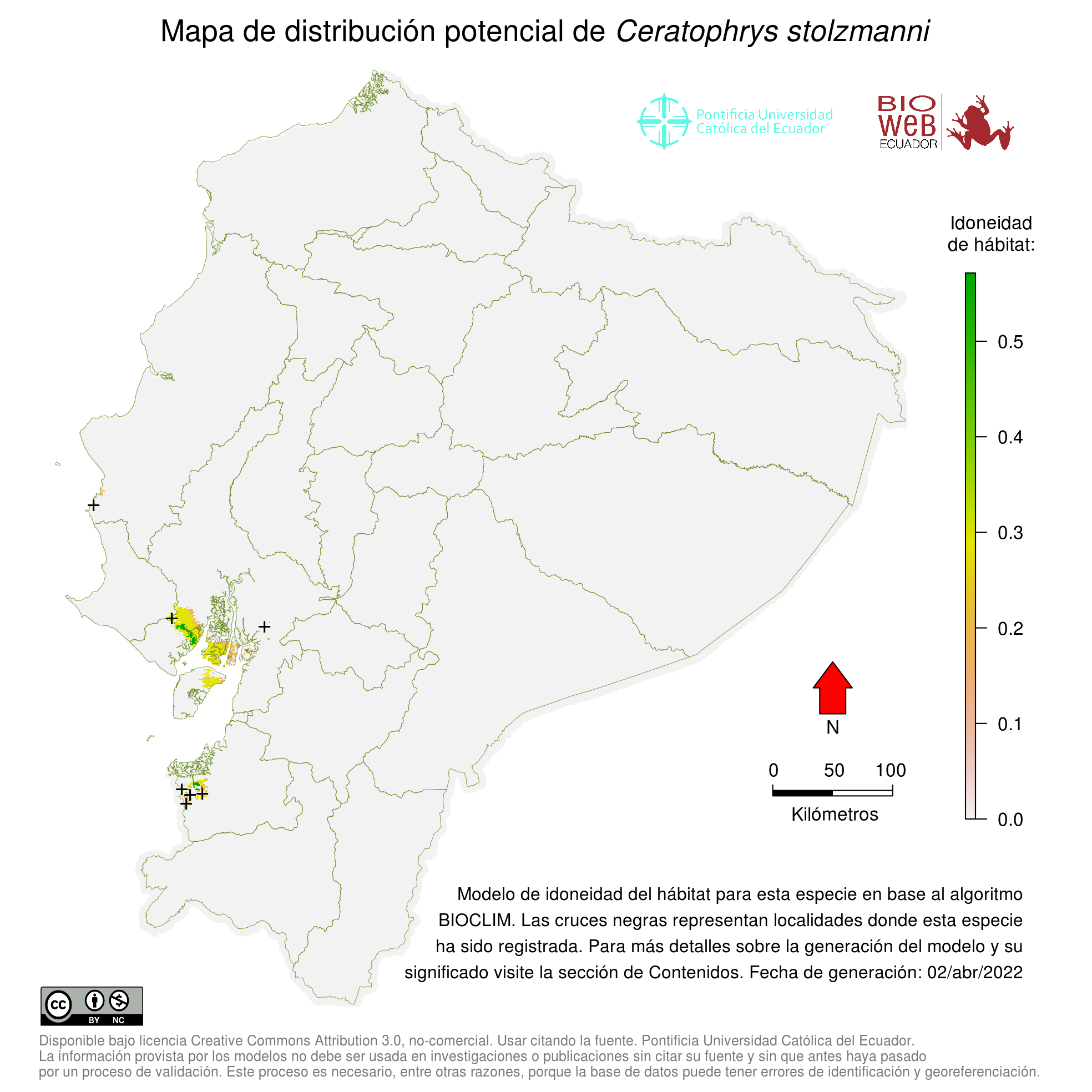
Distribution
Se distribuye en el suroccidente de Ecuador (Provincias Manabí, Santa Elena, Guayas y El Oro) y noroccidente de Perú (Departamento de Tumbes [localidad tipo = Tumbes]) (9).
Altitudinal Range
De 0 a 130 m sobre el nivel del mar
Taxonomy and Evolutionary Relationships
Información genética indica una relación cercana a Ceratophrys cornuta y Ceratophrys calcarata ( 13). Esta relación fue previamente sugerida, en base a caracteres morfológicos, por Lynch ( 6) quien propone el subgénero Stombus para las tres especies. Peters ( 5) reconoció dos subespecies: Ceratophrys stolzmanni de la localidad tipo en Perú (Tumbes, Departamento Tumbes) y Ceratophrys stolzmanni scaphiopeza de Ecuador (Cuatro Hermanitos, Provincia Guayas). La diferencia radicaría en que la piel de fondo del dorso y flancos de Ceratophrys stolzmanni es altamente pustular, mientras que la de Ceratophrys stolzmanni scaphiopeza es lisa. Sin embargo, se requiere de un estudio adicional para corroborar esta distinción, debido a que las diferencias se basan en pocos individuos y los métodos de preservación pueden alterar los caracteres usados para diferenciar las subespecies.
Etymology
El nombre específico es un patronímico para von Herrn Stolzmann, quién colectó los especímenes utilizados para la descripción (1).
Additional Information
Lynch ( 12) presenta una diagnosis osteológica y de caracteres externos para el género. Thomas y Thomas ( 10) reportan haber encontrado 15 cráneos y fragmentos de huesos de Ceratophrys stolzmanni en un depósito grande (~1 m de diámetro, 0.3 m de profundidad) de egagrópilas (restos no digeridos regurgitados) presuntamente de un búho, a 5 km de Puerto Pizarro (Departamento de Tumbes, Perú). Lynch ( 6) provee una ilustración del párpado en vista dorsal. Ron et al. ( 2) proveen fotografías ex situ de adultos y renacuajos. Valencia et al. ( 3) la incluyen en su guía de campo. Ortiz et al. ( 8) proveen fotografías de Ceratophrys stolzmanni in situ (Reserva Ecológica Militar Arenillas, El Oro, Ecuador); así como de un macho cantando, una pareja en amplexus y la variación ontogénica del renacuajo en cautiverio. También describen técnicas de manejo y reproducción ex situ; así como características y comportamientos del cortejo, amplexus, oviposición, puesta de huevos, eclosión y desarrollo del renacuajo ( 8). Santillana-Ortiz et al. ( 7) estudiaron la diferenciación de la placa del techo del gastrocele durante el desarrollo embrionario y lo comparan con otras especies de ranas de desarrollo rápido y lento. Székely et al. ( 14) proveen información acerca de los tiempos de desarrollo de los renacuajos relacionados a la disponibilidad de agua. Székely et al. ( 15) presentan información demográfica en base a esqueletocronología. Amador y Brito ( 16) proveen nuevos registros para la provincia de Guayas, Ecuador y extienden el rango altitudinal superior para la especie a 130 m. Székely et al. ( 17) proveen el primer análisis descriptivo-cuantitativo sobre su dieta en estado natural en Ecuador.



Summary Author
Diego A. Ortiz
Editor
Santiago R. Ron, Diego Paucar
Edition Date
2020-06-12T00:00:00
Update Date
2024-03-19T18:16:25.91
Literature Cited
Steindachner, F. 1882. Batrachologische Beiträge. Sitzungsberichte der Akademie der Wissenschaften in Wien. Mathematisch-Naturwissenschaftliche Klasse 85:188-194.PDF Ron, S. R., Bustamante, M. R., Coloma, L. A. y Mena, B. 2009. Sapos, Ecuador sapodiverso. Serie de Divulgación del Museo de Zoología. Centro de Biodiversidad y Ambiente, Pontificia Universidad Católica del Ecuador 10:256. Valencia, J., Toral, E., Morales, M., Betancourt, R. y Barahona, A. 2009. Guía de campo de anfibios del Ecuador. Fundación Herpetológica Gustavo Orcés, Simbioe. Maxigraf S. A., Quito 208. Rodríguez, L. O. y Duellman, W. E. 1994. Guide to the frogs of the Iquitos Region, Amazonian Perú. Asociación de Ecología y Conservación, Amazon Center for Environmental Education and Research and Natural History Museum, The University of Kansas. Lawrence, Kansas 22:1-80.PDF Peters, J. A. 1967. The generic allocation of the frog Ceratophrys stolzmanni Steindachner, with the description of a new subspecies from Ecuador. Proceedings of the Biological Society of Washington 80:105-112.PDF Lynch, J. D. 1982. Relationships of the frogs of the genus Ceratophrys (Leptodactylidae) and their bearing on hypotheses of Pleistocene forest refugia in South America and punctuated equilibria. Systematic Zoology 31:166-179. Santillana-Ortiz, J.D., Sáenz-Ponce, N., del Pino, E. 2012. The gastrocoel roof plate in embryos of different frogs. Differentiation 83: 62–66. Ortiz, D. A., Almeida-Reinoso, D. P., Coloma, L. A. 2013. Notes on husbandry, reproduction and development in the Pacific horned frog Ceratophrys stolzmanni (Anura: Ceratophryidae), with comments on its amplexus. International Zoo Yearbook 47:151-162. Frost, D. R. 2013. Amphibian Species of the World: an online reference. Version 5.6 (15 October, 2012). Base de datos accesible en http://research.amnh.org/vz/herpetology/amphibia/ American Museum of Natural History, New York, USA. Thomas, R. y Thomas, K. R. 1977. A small-vertebrate thanatocenosis fron northern Peru. Biotropica 9:131-132. Angulo, A., Coloma, L. A., Ron, S. R., Cisneros-Heredia, D. F. 2004. Ceratophrys stolzmanni. En: The IUCN red list of threatened species. Gland and Cambridge. (Consultado 2013). Lynch, J. D. 1971. Evolutionary relationships, osteology, and zoogeography of leptodactyloid frogs. Micellaneous publications, University of Kansas Museum of Natural History 53:1-238.Enlace Faivovich, J., Nicoli, L., Blotto, B. L., Pereyra, M. O., Baldo, D., Barrionuevo, J. S., Fabrezi, M., Wild, E. R., Haddad, C. F. B. 2014. Big, bad, and beautiful: phylogenetic relationships of the horned frogs (Anura: Ceratophryidae). South American Journal of Herpetology 9:207-227.PDF Székely, D., Denoël, M., Székely, P., Cogalniceanu, D. 2017. Pond drying cues and their effects on growth and metamorphosis in a fast developing amphibian. Journal of Zoology. Székely, D., Székely, P., Stănescu, F., Cogălniceanu, D., Sinsch, U. 2018. Breed fast, die young: demography of a poorly known fossorial frog from the xeric Neotropics. Salamandra 54: 37-44. Amador, L., Brito, G. 2013. Notes on the distribution and conservation of Ceratophrys stolzmanni (Steindachner, 1882) (Anura: Ceratophryidae) in Ecuador. Yachana 2: 123-126.Székely, D., Gaona, F., Székely, P., Cogalniceanu, D. 2019. What does a Pacman eat? Macrophagy and necrophagy in a generalist predator (Ceratophrys stolzmanni). PeerJ 7: e6406.
|
